Back ثنائي كلوريد ثنائي الكبريت Arabic دیسولفور دیکولورید AZB Chlorid sirný Czech Dischwefeldichlorid German Disulfur dichloride English Dusulfura duklorido Esperanto Dicloruro de disulfuro Spanish دیسولفور دیکلرید Persian Dirikkidikloridi Finnish Dikén-diklorid Hungarian
| Chlorure de soufre | |||

| |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | dichlorure de disoufre | ||
| No CAS | |||
| No ECHA | 100.030.021 | ||
| No CE | 233-036-2 | ||
| Apparence | liquide fumant, huileux, ambre à rouge, d'odeur âcre[1] | ||
| Propriétés chimiques | |||
| Formule | S2Cl2 | ||
| Masse molaire[2] | 135,036 ± 0,014 g/mol Cl 52,51 %, S 47,49 %, |
||
| Propriétés physiques | |||
| T° fusion | −77 °C[1] | ||
| T° ébullition | 138 °C[1] | ||
| Solubilité | dans l'eau : réaction[1] | ||
| Masse volumique | 1,7 g·cm-3[1] | ||
| T° d'auto-inflammation | 234 °C[1] | ||
| Point d’éclair | 118 °C (coupelle fermée)[1] | ||
| Pression de vapeur saturante | à 20 °C : 0,90 kPa[1] | ||
| Précautions | |||
| SGH[3] | |||
| H301, H314, H332, H400, EUH014 et EUH029 |
|||
| SIMDUT[4] | |||
  D1B, E, |
|||
| NFPA 704 | |||
| Transport | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
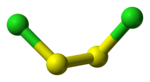
Le dichlorure de disoufre a pour formule S2Cl2. Il est aussi appelé (mono)chlorure de soufre, nom issu de sa formule empirique SCl. S2Cl2 a une structure pliée dans laquelle l'angle entre les plans Cla-S-S et S-S-Clb est d'environ 90°. Cette structure est gauche et est comparable à celle du peroxyde d'hydrogène H2O2. L'isomère de S2Cl2, S=SCl2, apparaît brièvement lors de l'exposition de S2Cl2 aux UV.
- MONOCHLORURE DE SOUFRE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE no 1272/2008 (16 décembre 2008)
- « Chlorure de soufre » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search